在烧结砖瓦原材料中最常见的硫酸盐矿物是石膏,偶尔也会发现重晶石(BaSO4)矿物。钙和钡的硫酸盐对砖瓦产品来讲是完全有害的矿物,因为这两种硫酸盐都是反应活性很强的矿物,在焙烧过程中都可能会与硅酸盐或铝硅酸盐矿物反应,成为含硫气体的来源。如果这类气体存在于制品内甚至于比排放到环境中更有害。石膏或多或少要溶解在搅拌水中,从而引发了干燥泛白或滞留在成品中造成后期泛霜的问题等。
在烧结砖瓦原材料中发现的天然石膏矿物有天然二水石膏(CaSO4•2H2O)及天然无水石膏(CaSO4)。天然二水石膏质地较软,故又称软石膏。天然无水石膏因质地较硬,故又称硬石膏。天然二水石膏(dihydrate gypsum)也称生石膏,是所有石膏相中最常见的一种,所以简称石膏。纯洁的石膏是透明无色或白色,但是在砖瓦原材料中的石膏因有砂、黏土矿物、碳酸盐矿物、有机质以及氧化铁等各种物质的混入和影响而呈灰色、褐色、赤色或灰黄色及淡红色等多种颜色。石膏矿常呈板状、叶片状、针状和纤维状晶形,少数呈柱状,有时也可见燕尾形的连生双晶。玻璃或丝绢光泽,解理面呈现出珍珠变彩。硬度2,性脆,密度2.30~2.33。略溶于水,温度为20℃时一升水可溶解2.6克石膏。当温度在32~34℃之间时,石膏的溶解度最大。表26给出了石膏的溶解度数据。石膏溶于盐酸但不起泡,具有很低的导热率。加热失水或完全脱水。
表26:CaSO4•2H2O在水中的溶解度
![]()
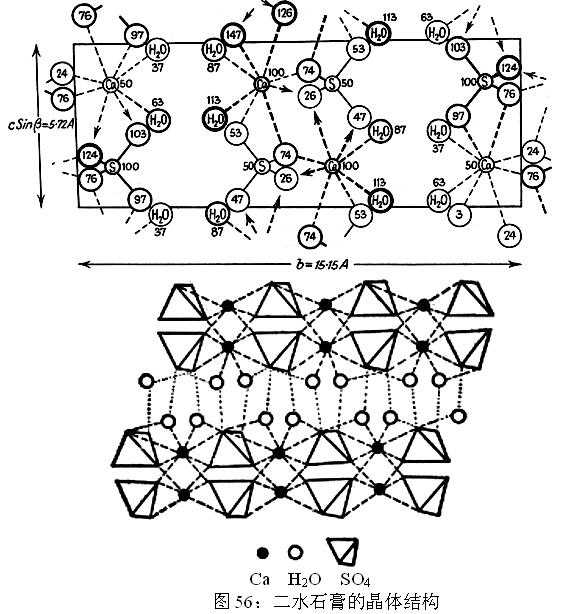
石膏的化学组成为CaSO4•2H2O,其中:CaO=32.56%;SO3=46.51%;H2O=20.93%。Ca可少量被Sr代替。二水石膏属单斜晶系,晶胞尺寸为:a0=5.76Å;bo=15.15Å;co=6.28Å;β=115º56′。图56表示了二水石膏的晶体结构。
从图56中可以看出,二水石膏具有由Ca2+离子连接[SO4]2—四面体而构成双层的结构层,H2O分子则分布在双层结构层之间,Ca2+的配位数为8,它除了与相邻的四个[SO4]2—四面体中的六个O2—相连接外,还与二个H2O分子连接。结构层平面为[010],所以二水石膏常呈[010]的板状形态,并在这个面上有极完全的解理。
二水石膏的晶形如图57所示。图57表明石膏在结晶生长时,一般向a轴和c轴发展,形成对[010]晶面发育的板状晶体,有时也只向c轴生长延长,这时可形成柱状或针状晶体。由于二水石膏[010]面解理完全,所以在显微镜下常看到菱形薄板状、柱板状或针状晶体。必须提到的是:二水石膏的晶形也常受到微量杂质、溶液的性质、pH值及温度等因素的影响而变化。但是不同晶形的二水石膏,其折射率是一定的。

图57:二水石膏的晶形
二水石膏加热时失去结晶水,变成半水石膏和无水石膏。上述石膏相的化学组成和晶形如表27所示。
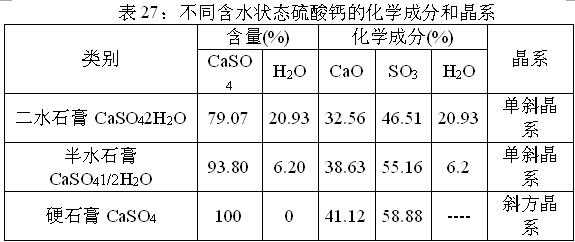
无水石膏(硬石膏)的化学组成CaSO4,常含少量Sr、Mg、Si、Al等杂质。斜方晶系,晶体呈柱状或厚板状,常为致密块状或粒状集合体。白色,含杂质时为灰白、浅灰、灰黑色,偶见无色透明晶体。玻璃光泽,解理面呈珍珠光泽。硬度3.0~3.5,性脆,密度2.8~3.1。硬石膏较二水石膏难溶于水,但在空气中易水化成二水石膏,且体积增大。硬石膏主要为盐湖中化学沉淀作用的产物,与二水石膏、石盐等共生,往往地表及浅部变为二水石膏,而深部仍为硬石膏。
应当指出,当二水石膏加热脱水时,由于加热的程度及条件不同,脱水石膏的结构和特性也不同。二水石膏在加热过程中生成的不同变体及其形成与转化的条件如图58所示。
二水石膏的差热分析曲线表明,在140℃左右有一个吸热峰,这时二水石膏失去一个半分子的水,接着在190℃左右又有一个吸热峰,这时又失去另外半个分子的水,变为脱水半水石膏(或称Ⅲ型无水石膏)。然后在360℃左右有一个放热峰,这时Ⅲ型无水石膏转变为Ⅱ型无水石膏(或称可溶性石膏)。上述Ⅱ型CaSO4在500~750℃的温度范围内转变成不溶性硬石膏(亦称Ⅰ型CaSO4),此时无显著热效应发生,即在此温度下不发生相变,只是结晶体变得更紧密和稳定,密度达2.99,难溶于水,凝结很慢,甚至完全不凝结。但是,当加入某些激发剂时,则可使它水化,转化为二水石膏。例如加入5%的硫酸钠或硫酸氢钠与1%的铁矾的混合物;1~5%的石灰与少量半水石膏
的混合物;3~8%经800~900℃煅烧过的白云石;10~15%的碱性粒状矿渣;2%的硫酸铝或硫酸锌等。这些激发剂的作用机理是:CaSO4具有组成络合物的能力,在有水和盐存在时,CaSO4表面生成把稳定的复杂水化物(盐•mCaSO4•nH2O),然后此水化物又分解为含水盐类和二水石膏。
该变化过程的反应可表示如下:
mCaSO4+盐•nH2O(激发剂)=盐•mCaSO4•nH2O(复盐)
盐•mCaSO4•nH2O= mCaSO4•2H2O+盐•(n-2m)H2O
版权所有:【河南欧帕工业机器人有限公司】
本站所有内容受知识产权保护 未经许可严禁转载、复制或建立镜像
中心地址:河南省郑开大道官渡组团 联系电话:0371-60863533
豫ICP备14017777号-3 营业执照 河南省互联网违法和不良信息举报中心

